Portal Kudus - Inilah cara menghitung dan contoh soal fraksi mol dan jawabannya rumus dan pembahasan fraksi mol terlarut dan pelarut.
Bagi kalian yang bingung dan mencari soal latihan cara menghitung molalitas dan fraksi mol, simak artikel ini hingga selesai.
Artikel ini akan menyajikan contoh soal molalitas dan fraksi mol dan penjelasannya lengkap guna menjadi panduan agar membantu belajar kalian.
Sekalipun sudah ada kunci jawaban semacam ini, tentu akan lebih baik lagi jika para siswa terlebih dahulu mencoba untuk mengerjakannya.
Adanya kunci jawaban ini diharapkan bisa menjadi sebuah referensi atau bahan evaluasi dalam proses belajar mengajar.
Sebagaimana yang dilansir tim PortalKudus dari berbagai sumber berikut ini contoh soal molalitas dan fraksi mol dan pembahasannya.
1.Sebanyak 30 gram urea C₆H₁₂O₆ (Mr = 60 g/mol) dilarutkan ke dalam 100 gram air. Hitunglah molalitas larutan.
Jawaban :
Diketahui: massa urea = 30 gram
Mr = 60 g/mol
massa pelarut = 100 gram = 0,1 kg

Jadi, molalitas larutan 30 gram urea C₆H₁₂O₆ adalah 5 m.
2. Berapakah kemolalan dari larutan 10% (w/ w) NaCl (Mr NaCl = 58,5) (w/ w = persen berat)?
Pembahasan: Larutan 10% (w/ w) → w berasal dari kata weight.
Diketahui: % = 10%
Mr = 58,5 g/mol
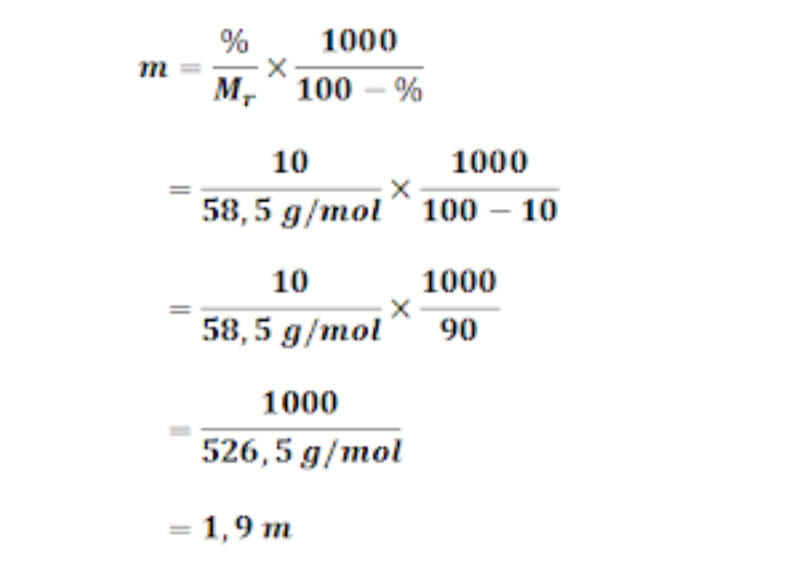
Jadi, larutan 10% (w/ w) NaCl memiliki konsentrasi 1,9 m.
3. Berapakah fraksi mol dan persen mol yang dihasilkan pada setiap komponen dari campuran 0,2 mol O₂ dan 0,5 mol N₂?
Jawaban;
Diketahui:mol O₂ = 0,2 mol
mol N₂ = 0,5 mol

% mol O₂ = 0,29 × 100% = 29%
% mol N₂ = 0,71 × 100% = 71%
Jadi, fraksi mol O₂ adalah 0,29 dan fraksi mol N₂ adalah 0,71, sedangkan persen mol O₂ adalah 29% dan persen mol N₂ adalah 71%.
4.Berapakah molalitas larutan yang mengandung 4 gr NaOH (Ar Na = 23 gr/mol, Ar O = 16 g/mol, dan Ar H = 1 gr/mol) terlarut dalam 250 gr air?
Penyelesaian:
Diketahui:
massa NaOH = 4 gr
Ar Na = 23 gr/mol
Ar O = 16 g/mol
Ar H = 1 gr/mol
massa air = 250 gr = 0,25 kg
Ditanyakan: m = ?
Jawab:
Mr.NaOH = 40 gr/mol
jumlah mol NaOH = massa/Mr
jumlah mol NaOH = 4 gr/(40 gr/mol)
jumlah mol NaOH = 0,1 mol
m = jumlah mol/p
m = 0,1 mol /0,25 kg
m = 0,4 m
5.Berapakah molalitas dari larutan HCl 37% (w/w)? (Ar H = 1 g/mol, Ar Cl = 35,5 g/mol)
Penyelesaian:
Diketahui:
massa HCl = 37%
Ar H = 1 g/mol
Ar Cl = 35,5 g/mol
Ditanyakan: m = ?
Jawab:
Mr.HCl = 36,5 gr/mol
misalkan massa larutan adalah 100 gr maka massa HCl yakni:
massa HCl = 37% x 100 gr
massa HCl = 37 gr
massa pelarut = massa larutan – massa HCl
massa pelarut = 100 gr – 37 gr
massa pelarut = 63 gr = 0,063 kg
jumlah mol HCl = massa/Mr
jumlah mol HCl = 37 gr /(36,5 gr/mol)
jumlah mol HCl = 1,01 mol
m = jumlah mol/ massa pelarut
m = 1,01 mol /0,063 kg
m = 16,03 m
6.Tentukan molalitas larutan yang dibuat dengan melarutkan 12 gram urea CO(NH2)2 dalam 250 gram air.
Penyelesaian:
Diketahui:
massa urea = 12 gr
Mr Urea= 60 g/mol
massa pelarut = 250 gr = 0,25 kg
Ditanyakan: m = ?
Iklan
Jawab:
jumlah mol Urea = massa/Mr
jumlah mol Urea = 12 gr /(60 g/mol)
jumlah mol Urea = 0,2 mol
m = jumlah mol/ massa pelarut
m = 0,2 mol /0,25 kg
m = 0,8 m
7.Berapa molalitas larutan alkohol yang mengandung 23 % massa etanol (Mr = 46)?
Jawab:
Diketahui:
massa etanol = 23 %
Mr etanol = 46 g/mol
Ditanyakan: m = ?
Penyelesaian:
misalkan massa larutan alkohol adalah 100 gr maka massa etanol yakni:
massa etanol = 23% x 100 gr
massa etanol = 23 gr
massa pelarut = massa larutan – massa etanol
massa pelarut = 100 gr – 23 gr
massa pelarut = 77 gr = 0,077 kg
jumlah mol etanol = massa/Mr
jumlah mol etanol = 23 gr /(46 g/mol)
jumlah mol etanol = 0,5 mol
m = jumlah mol/ massa pelarut
m = 0,5 mol /0,077 kg
m = 6,49 m
8.Hitung kadar (% massa) glukosa dalam larutan glukosa 2 molal.
Penyelesaian:
Diketahui:
m = 2 molal = 2 mol/kg = 0,002 mol/gr
Mr glukosa = 180 gr/mol
Ditanyakan: massa glukosa (%) = ?
Jawab:
mol glukosa = massa/Mr
mol glukosa = massa glukosa/(180 gr/mol)
mol glukosa = massa glukosa x 0,005 mol/gr
Substitusi mol glukosa ke persamaan berikut:
m = mol glukosa/massa pelarut
0,002= massa glukosa x 0,005/massa pelarut
o,oo2/o,oo5 = massa glukosa/massa pelarut
2/5 = massa glukosa/massa pelarut
Jadi perbandingan massa glukosa : massa pelarut = 2:5, sedangkan perbandingan massa glukosa : massa larutan = 2:7.
Maka,
% massa glukosa = (massa glukosa/massa larutan) x100%
% massa glukosa = (2/7) x 100%
% massa glukosa = 28,57 %
Soal 6
Berapakah molalitas larutan yang mengandung 8 gram NaOH (Ar Na = 23 gr/mol, Ar O = 16 g/mol, dan Ar H = 1 gr/mol) terlarut dalam 250 gr air?
Pembahasan
Diketahui:
Massa NaOH = 8 gr
Ar Na = 23 gr/mol
Ar O = 16 g/mol
Ar H = 1 gr/mol
massa air = 250 gr = 0,25 kg
Ditanya: Molalitas (m)….?
Jawab:
Mr.NaOH = 40 gr/mol
Jumlah mol NaOH = massa/Mr
Jumlah mol NaOH = 8 gr/(40 gr/mol)
Jumlah mol NaOH = 0,2 mol
m = jumlah mol/p
m = 0,2 mol /0,25 kg
m = 0,8 m
Demikian informasi terkait contoh kumpulan soal molalitas dan fraksi mol, rumus dan hitunglah molalitas dan fraksi mol.***
*Disclaimer
1. Konten ini dibuat untuk siswa atau orang tua dalam proses evaluasi belajar dalam menemukan soal dan kunci jawaban.
2. Artikel ini tidak mutlak menjamin kebenaran jawaban.
3. Jawaban bersifat terbuka, dimungkinkan bagi guru atau siswa mengeksplorasi jawaban lain yang lebih baik.





