Portal Kudus - Berikut kumpulan soal fraksi mol terlarut dan pelarut lengkap dengan pembahasan, contoh soal Kimia kelas 12 SMA.
Kumpulan soal fraksi mol terlarut dan pelarut lengkap dengan pembahasan, contoh soal Kimia kelas 12 SMA berikut ini dapat dijadikan oleh gurun sebagai bahan referensi membuat soal ulangan.
Selain itu, kumpulan soal fraksi mol terlarut dan pelarut lengkap dengan pembahasan, contoh soal Kimia kelas 12 SMA bisa digunakan siswa untuk mengasah kemampuan atau pemahaman mengenai materi tersebut.
Simak kumpulan contoh soal fraksi mol dan pembahasannya terbaru tahun 2022 berikut ini yang dilansir Portal Kudus dari berbagai sumber.
Baca Juga: Ekuitas dalam Akuntansi Adalah Apa? Simak Penjelasan Ekuitas dalam Akuntansi di Sini
Pengertian Fraksi Mol
Seperti yang diketahui konsentrasi larutan dapat dinyatakan dalam :
1. Fraksi Mol
2. Persen Berat
3. Molalitas (m)
4. Molaritas (M)
5. Normalitas (N)
Konsentrasi larutan sangat berkaitan erat dengan perbandingan zat terlarut dan pelarut. Salah satu untuk menyatkan hubungan tersebut adalah : fraksi mol.
Fraksi mol adalah hubungan yang berkaitan dengan perbandingan jumlah mol zat terlarut atau pelarut terhadap jumlah mol larutan (jumlah mol pelarut + jumlah mol terlarut).
Rumus Fraksi Mol
Hal yang perlu kita ketahui bahwa fraksi mol total selalu bernilai satu dan disamping itu fraksi mol tidak memiliki satuan. Untuk menyatkan atau menotasikan fraksi mol digunakan simbol X.
Baca Juga: KUMPULAN Contoh Soal Hukum Coulomb dan Jawabannya untuk Latihan Soal Fisika Kelas 12 SMA
Berdasarkan penjelasan di atas dan pengertian dari fraksi mol, fraksi mol dapat dirumuskan sebagai berikut:

Contoh Soal Fraksi Mol
1. Sebuah larutan terdiri dari 3 mol zat A, 3 mol zat B, dan 4 mol zat C. Hitung fraksi mol dari masing – masing zat tersebut ?
Pembahasan:
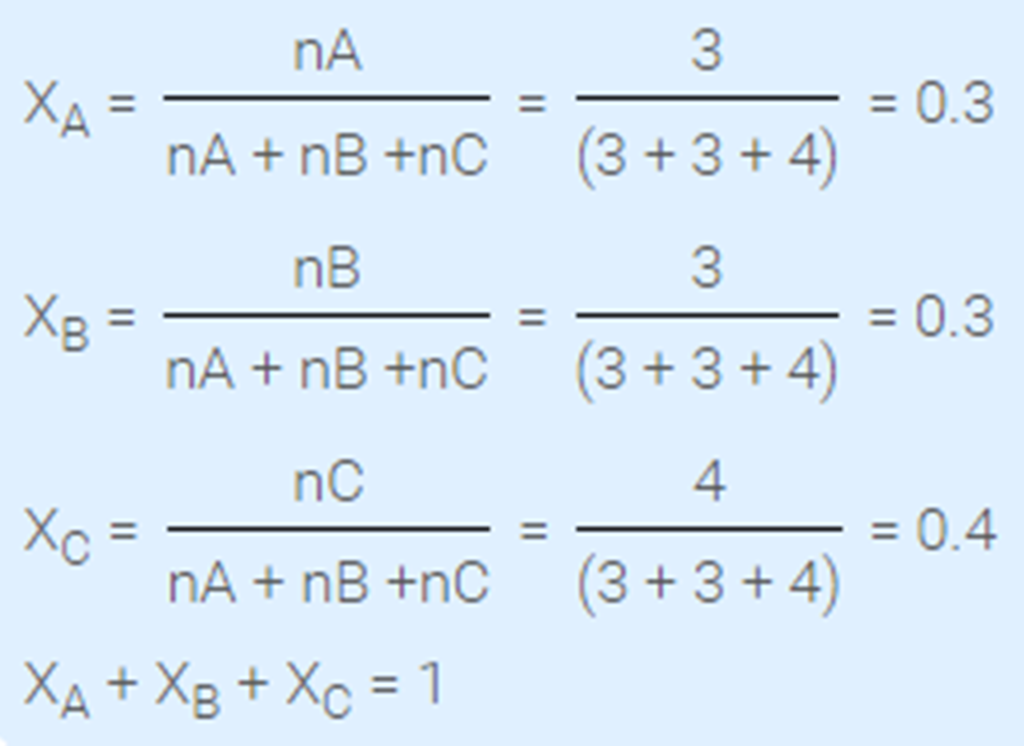
2. Terdapat sebuah larutan yang terdiri dari 2 mol zat A, 3 mol zat B, dan 5 mol zat C. Hitunglah masing-masing fraksi mol dari zat tersebut ?
Pembahasan:
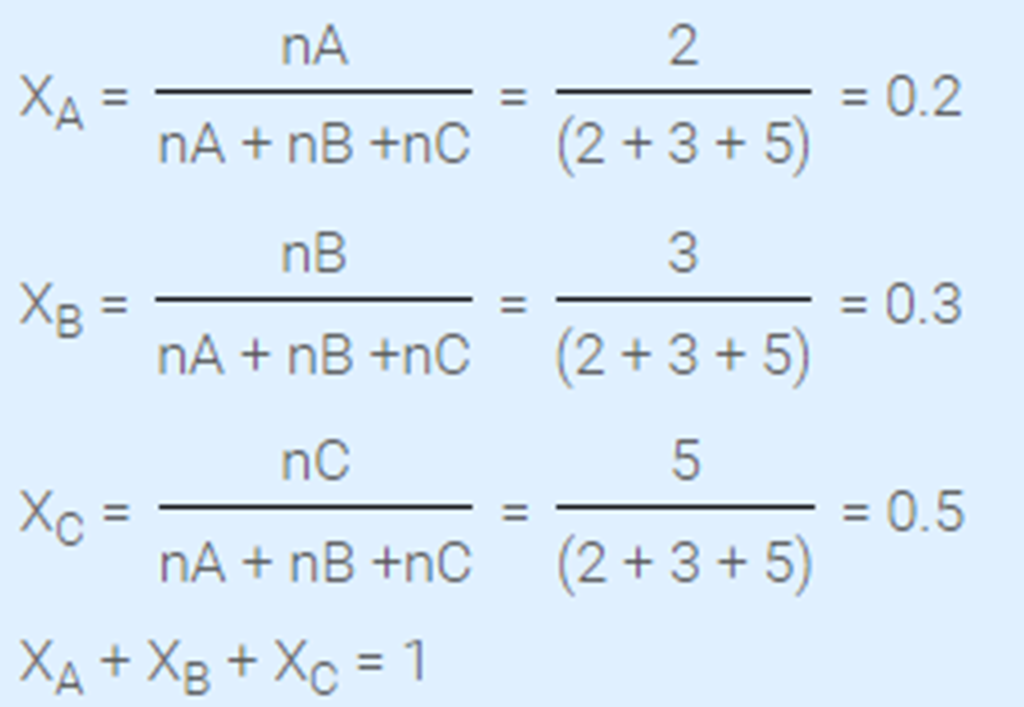
3. Fraksi mol urea 10% (Mr = 60) dalam pelarut air murni adalah...
A. 0,032
B. 0,034
C. 3,2
D. 3,4
E. 0,32
Pembahasan:
Pernyataan urea 10% menyatakan bahwa 100 gram larutan mengandung 10 gram urea.
Dengan demikian bisa kita dapatkan zat pelarut:
Massa larutan = massa terlarut + massa pelarut
100 gram = 10 gram + massa pelarut
massa pelarut = 100 gram - 10 gram
massa pelarut = 90 gram

4. Hitunglah fraksi mol etanol dan fraksi mol air dari 27,6 gram etanol C2H5OH yang dilarutkan dalam 54 gram H2O (Ar C = 12, H = 1, O = 16)!
Pembahasan:
Ar C = 12
Ar H = 1
Ar O = 16
Mr C2H5OH = (2 x Ar C) + (5 x Ar H) + Ar O + Ar H
Mr C2H5OH = 24 + 5 + 16 + 1
Mr C2H5OH = 46 gram/mol
Mr H2O = (2 x Ar H) + Ar O
Mr H2O = 2 + 16
Mr H2O = 18 gram/mol
massa C2H5OH = 27,6 gram
massa H2O = 54 gram

5. Hitunglah nilai fraksi mol etanol (Mr = 46) dalam larutan etanol 46% massa?

6. Fraksi mol larutan 36 gram glukosa (Mr = 180) dalam 90 gram air (Mr = 18) adalah....
A. 0,960
B. 0,400
C. 0,040
D. 0,038
E. 0,004
Pembahasan:

Demikian kumpulan contoh soal fraksi mol dan pembahasannya terbaru 2022. Semoga bermanfaat.***





